原子吸收光谱仪的结构及详细原理(上)

(上)篇包括原子吸收光谱分析方法的历史、原子吸收光谱分析的理论基础以及原子吸收的测量和数据分析。
(下)篇包括原子吸收光谱仪的结构和详细原理
原子吸收光谱法:被测元素基态原子在蒸汽状态下,外层电子由基态跃迁至激发态, 对光源发出的原子特征波长光辐射进行吸收, 引起特征波长光辐射的透射光强度减弱。原子吸收光谱法是基于此建立起的元素定量分析的方法,它是测定痕量和超痕量元素的有效方法之一。
棱镜实验
1666年,爱思考的牛顿先生发现,太沙巴滚球官网入口经过棱镜后被分成了华丽丽的彩色光带,他把这条光带称为光谱。

1802年,Wollaston发现了光谱中的黑线,但没给出科学的解释。
1814年,爱观察的Fraunhofer再次观察到了太沙巴滚球官网入口谱中的黑线,他在小黑屋内将一块火石玻璃棱镜放置在经纬仪前,让太沙巴滚球官网入口通过小缝投射到棱镜上,用经纬仪上的望远镜观察光谱时看到了很多条黑度不等的黑线密集在光谱上(这大概就是传说中五彩斑斓的黑)。

其中有两条最强的紧靠在一起的黑线,用字母D予以标记。他测定未分辨的D线的平均波长为588.7nm,与现在的精确值589.2nm已经非常接近。
Kirchhoff和Bunsen的实验
真正对原子吸收光谱的产生做出透彻解释的是后来的Bunsen和Kirchhoff。
他们进行的钠光谱中谱线自蚀的实验,是历史上用原子吸收光谱进行定性分析的第一个例证。
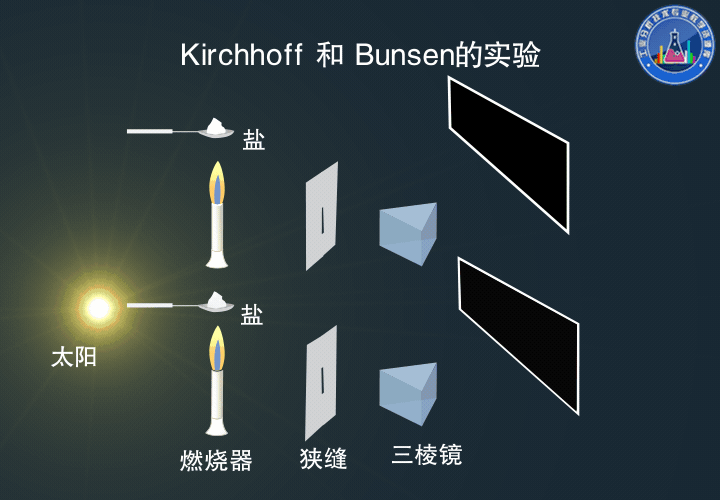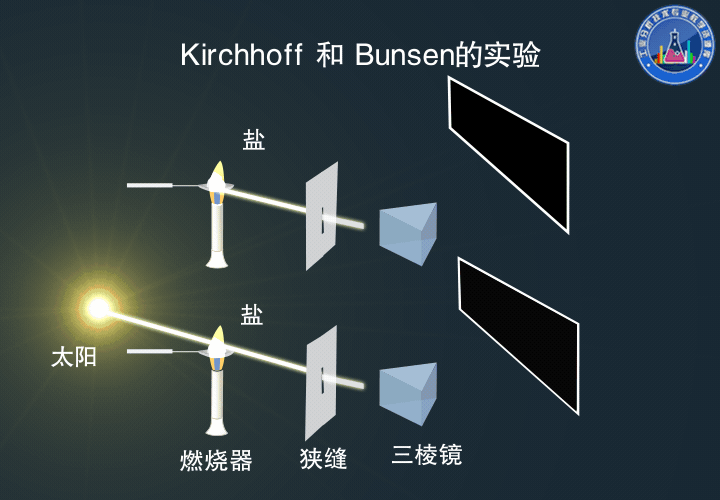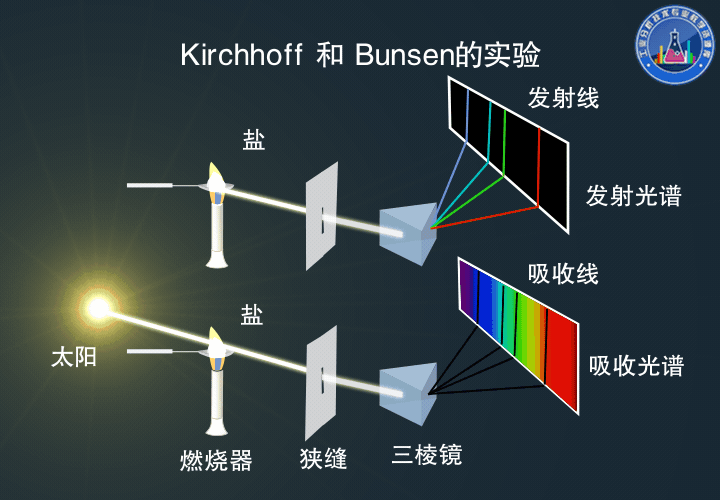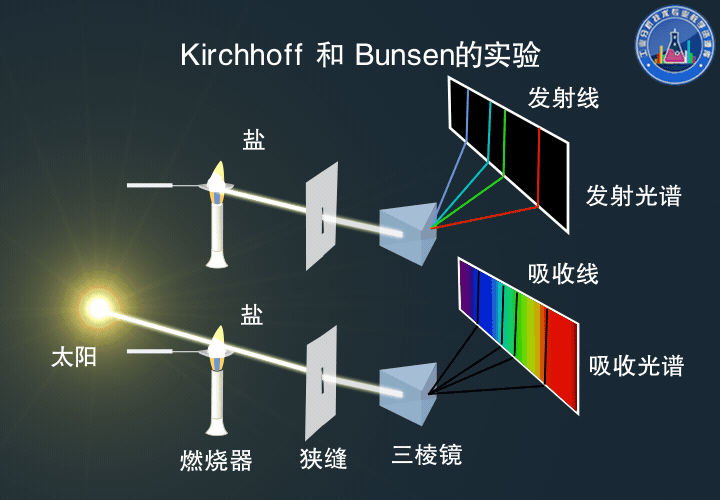
下:光束通过加热的金属盐后,观察到Fraunhofer吸收线
原子结构
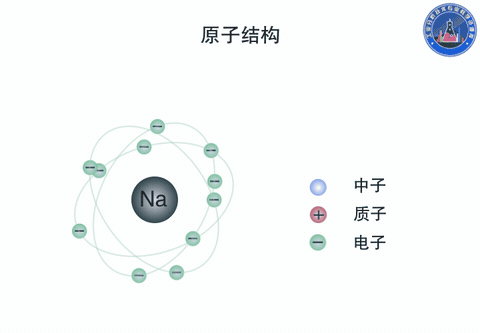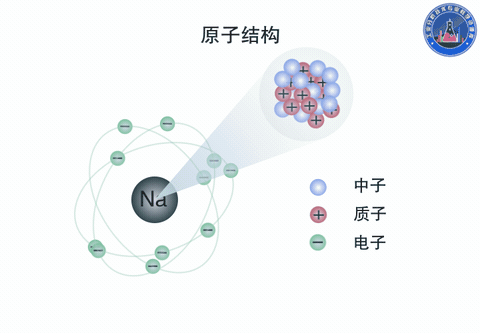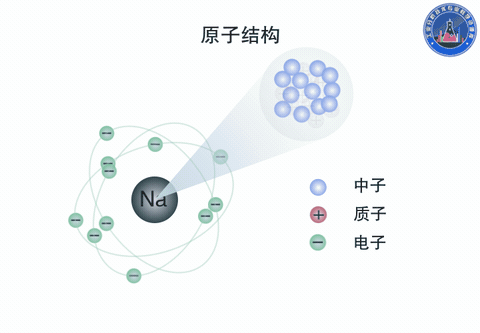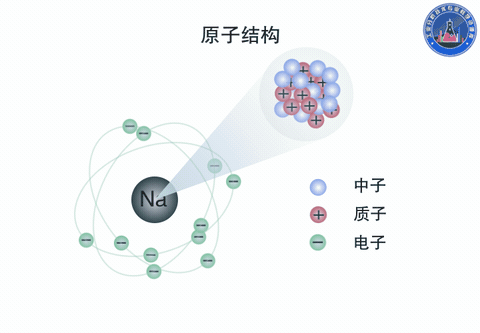
原子由原子核和核外电子组成。原子核是原子的中心体,由质子和中子构成,带正电。电子带负电,总的负电荷数与原子核的正电荷数相等。电子沿核外的圆形或椭圆形轨道围绕着原子核运动,同时又有自旋运动。
原子跃迁和能级图
电子由于具有不同的能量,就按照各自不同的轨道围绕原子核运转,即能量不同的电子处于不同的相应等级。
电子从基态跃迁到能量最低的激发态(称为第一激发态)时要吸收一定频率的光,这种谱线称为共振吸收线;当它再跃迁回基态时,则发射出同样频率的光(谱线),这种谱线称为共振发射线(它们都简称共振线)。

原子跃迁和激发
基态原子吸收一定频率的辐射能量,外层电子由基态跃迁到第一激发态或者更高激发态,产生共振吸收线,生成原子吸收光谱。
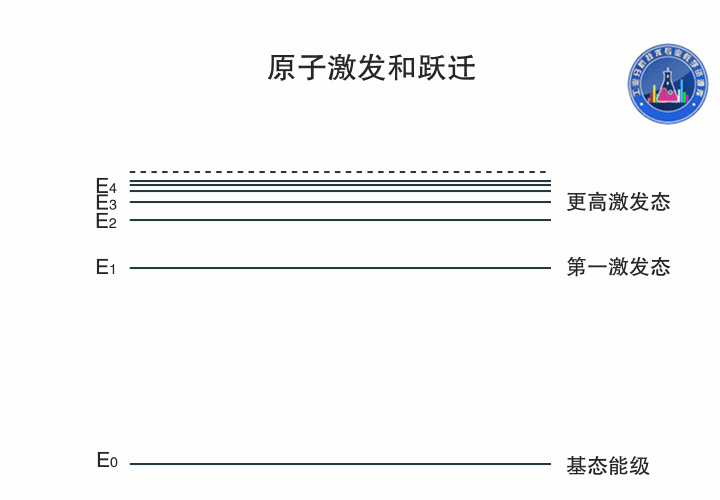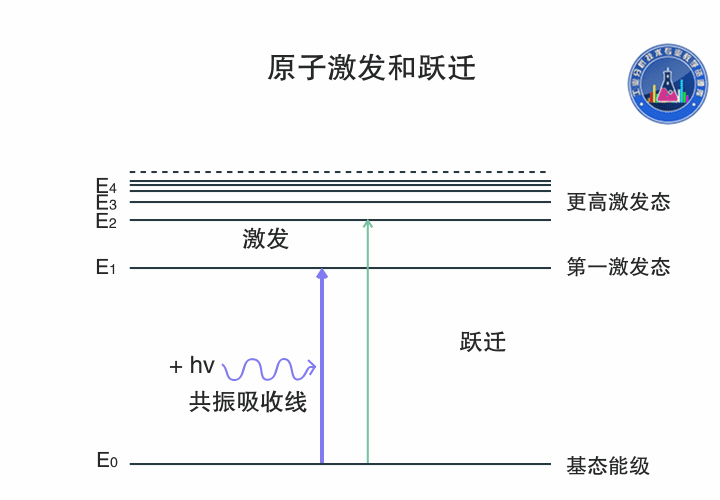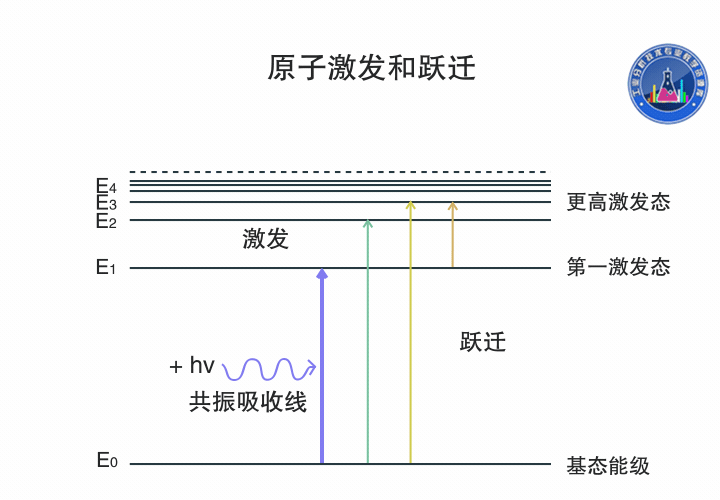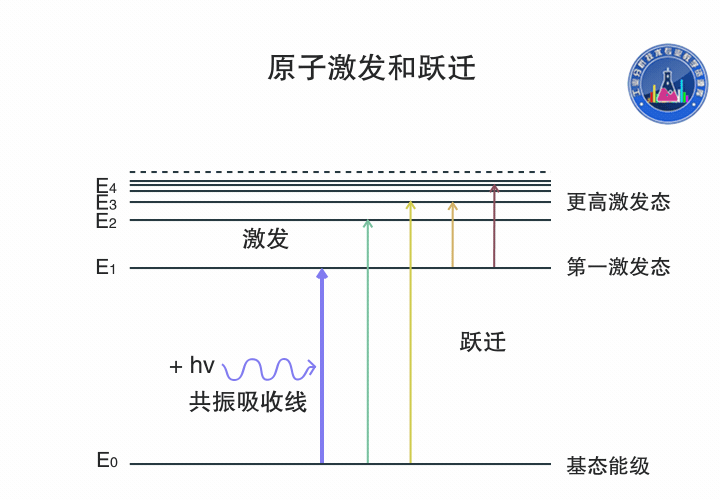
图中氢原子的电子可以通过吸收不同频率的辐射能量在各个能级间跃迁。
朗伯-比尔定律
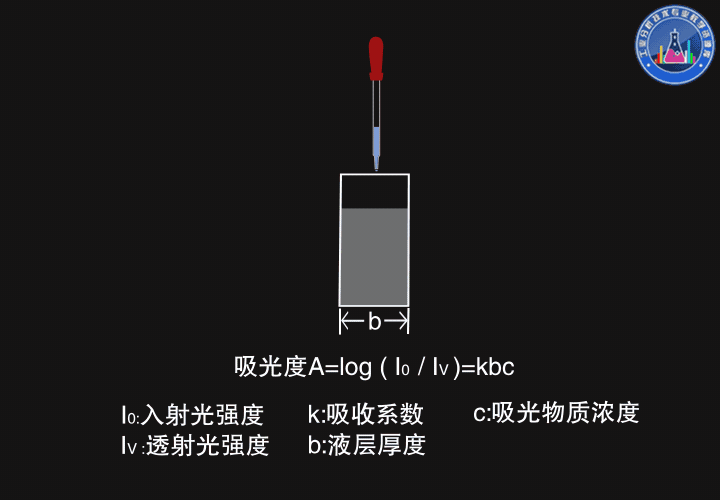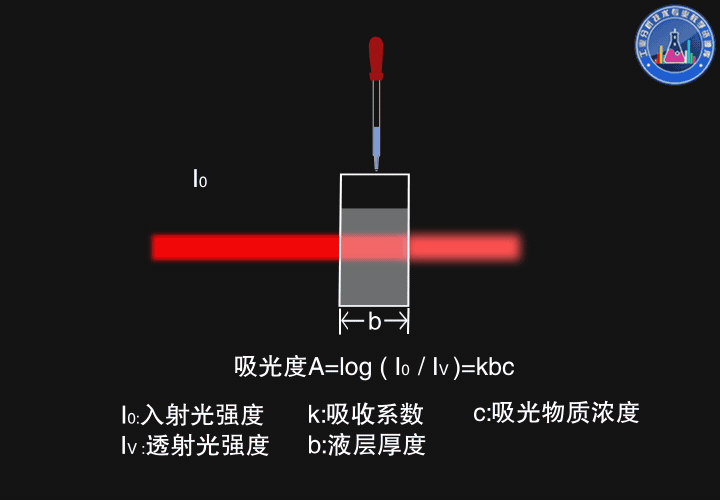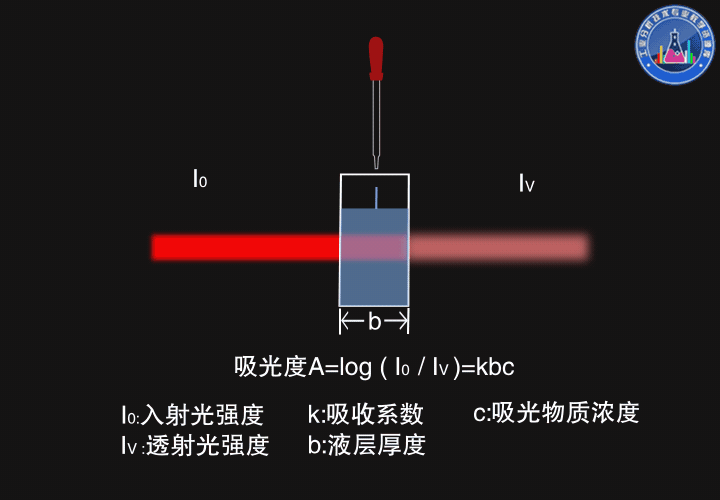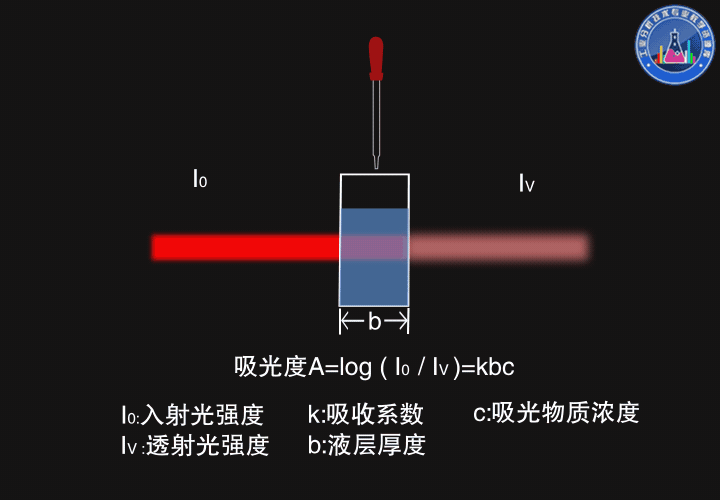
一束强度为I0的光通过厚度为b的原子蒸气,部分光被吸收,部分光被透过,透射光的强度Iν服从朗伯-比尔定律(Lambert-Beer law),吸光度A=log(I0/Iν)=kbc
如图所示,厚度变大时,透射光强度变弱,吸光度变大。

当浓度变大时,透射光强度也变弱,吸光度变大。
原子吸收光谱的谱线轮廓
原子结构简单,理论上应产生线状光谱吸收线,但实际上用强度为I0的不同频率辐射光照射时,获得的是峰形吸收,所得曲线为吸收线轮廓。
原子吸收光谱线占据着相当窄的频率范围,有一定的宽度,通常用吸收线的中心频率或中心波长与吸收线的半宽度来表示吸收线轮廓特征。
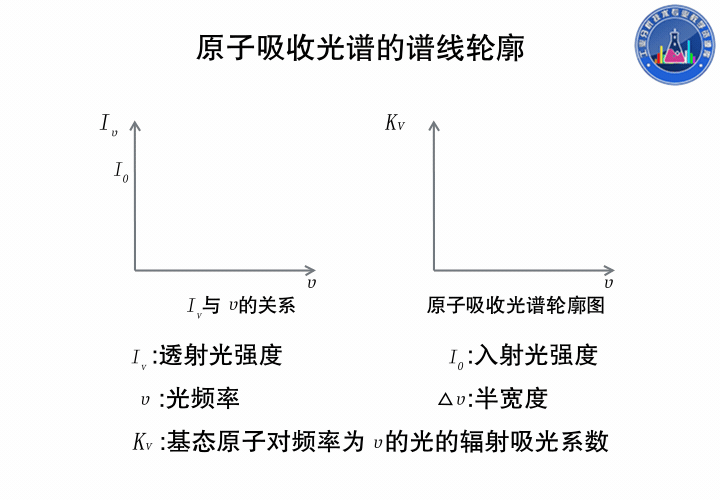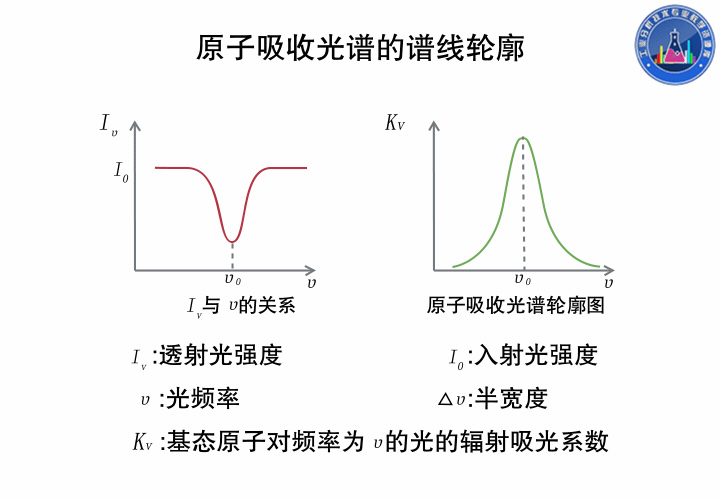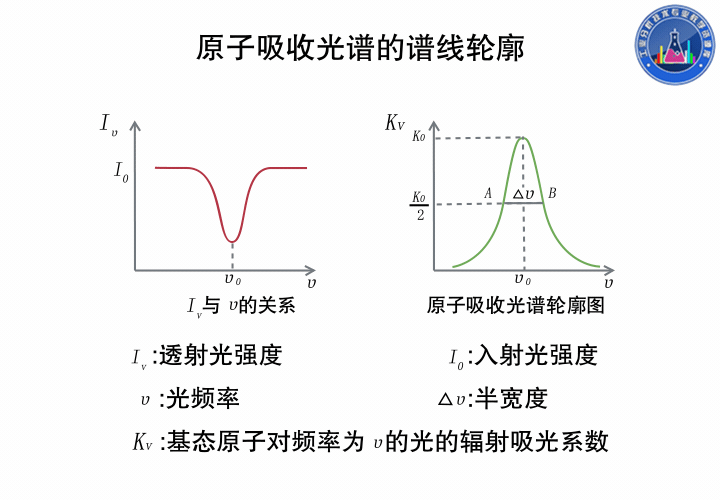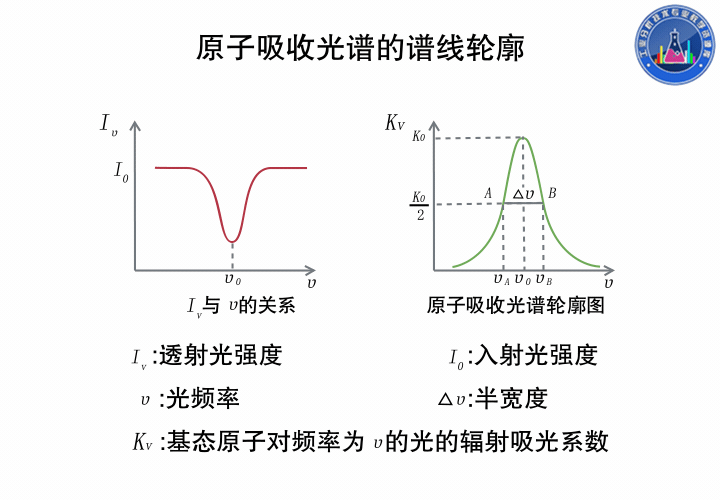
上图中,左边是透射光强度和光的频率的关系,右边是与之对应Kv与ν的关系。
吸收系数Kv是基态原子对频率为ν的光的辐射吸收系数,它随光源的辐射频率ν而改变,这是由于物质的原子对不同频率的光的吸收不同。
中心频率ν0指最大吸收系数对应的频率,由原子能级决定。
半宽度Δν0是指吸收系数极大值一半处,谱线轮廓上两点之间频率(波长)的距离,大约在10-3到10-2nm之间。
积分吸收测量法
在吸收线轮廓内,以吸收系数对频率积分称为积分吸收,积分得的结果是吸收线轮廓内的总面积,它表示原子蒸气吸收的全部能量。
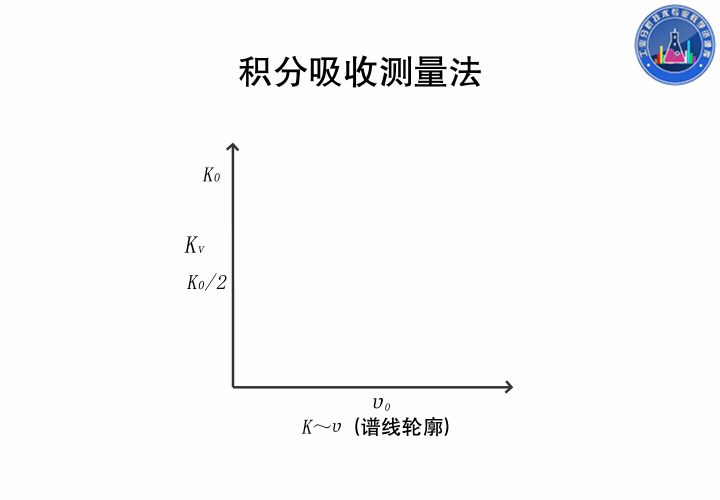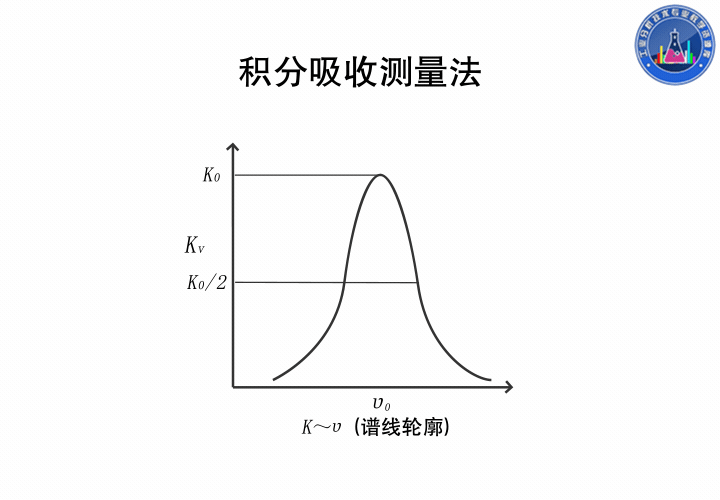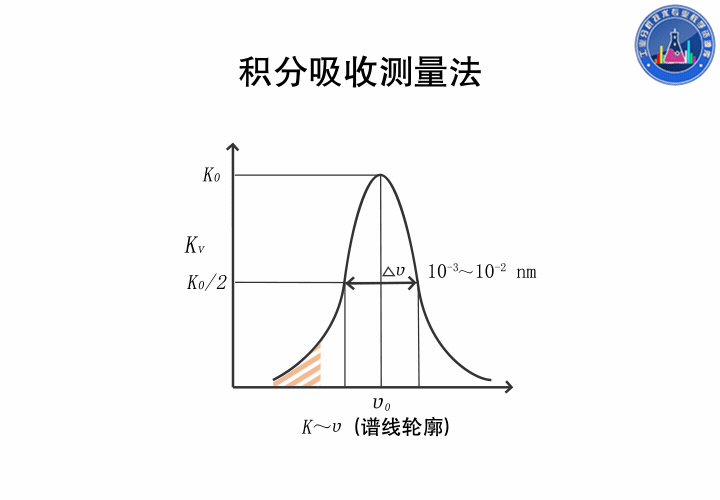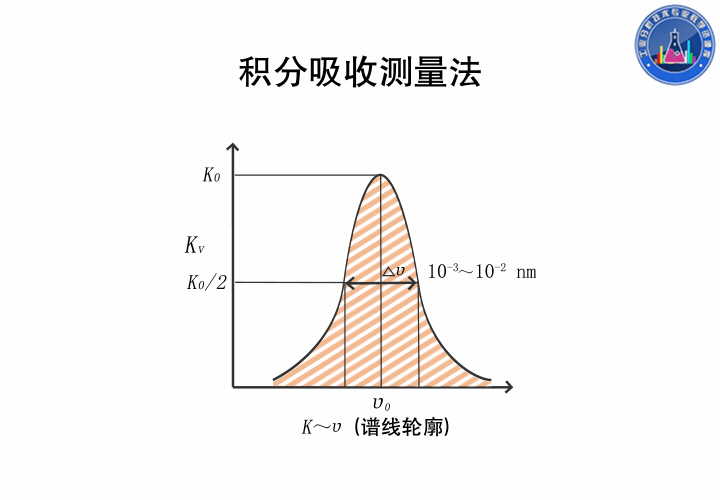
这是一种绝对测量方法,理论上,积分吸收与原子蒸气中吸收辐射的基态原子数成正比,若能测得积分吸收,就能求出原子浓度,但吸收线半宽度仅为10-3nm,现在的分光装置无法实现。
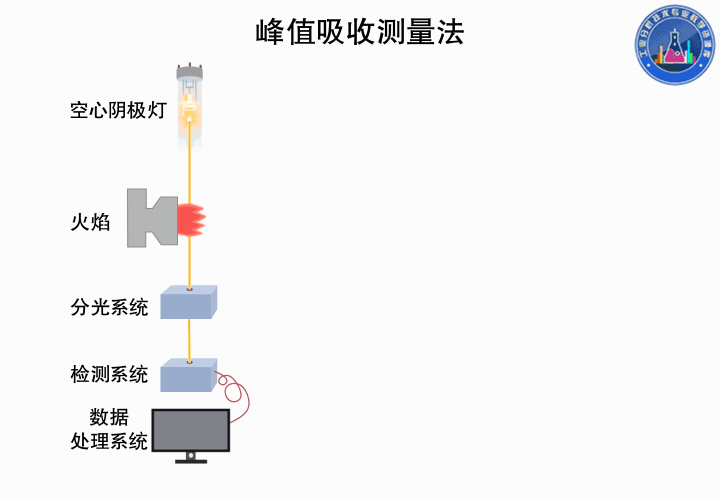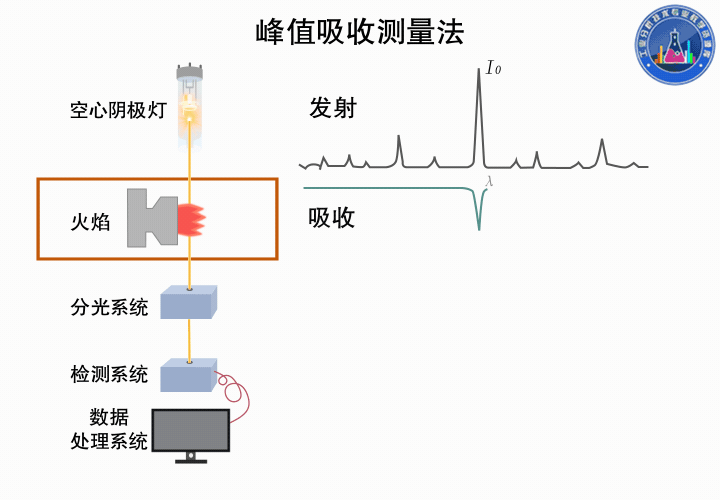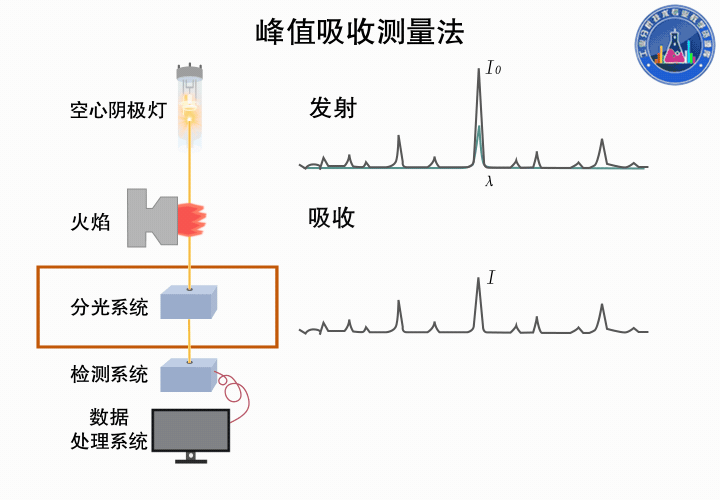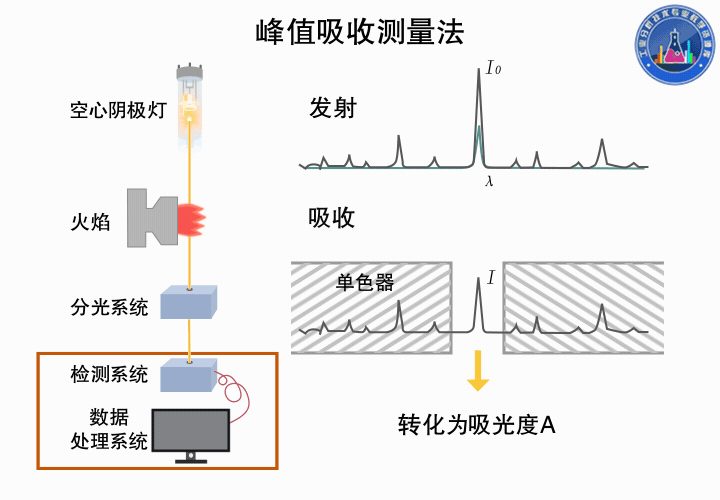
峰值吸收测量法
吸收线中心频率处的吸收系数Kn为峰值吸收系数,简称峰值吸收。
1955年Walsh提出在温度不太高的稳定火焰条件下,峰值吸收与火焰中被测元素的基态原子浓度也成正比,因此可用峰值吸收代替积分吸收。前提是采用锐线光源,即发射线半宽度比吸收线半宽度小得多的光源(例如空心阴极灯),并且发射线的中心与吸收线中心一致。
下图所示为峰值吸收测量的过程: